第一批医用耗材编码公示耗材管理持续规范化
来源:华体汇app入口 发布时间:2024-04-23 17:27:00据《国家医疗保障局关于印发医疗保障标准化工作指导意见的通知》(医保发〔2019〕39号)有关要求
据《国家医疗保障局关于印发医疗保障标准化工作指导意见的通知》(医保发〔2019〕39号)有关要求,医保局组织并且开展了医保医用耗材信息维护和审核工作,现将第一批医用耗材信息予以公示;经公示无异议后,第一批医用耗材信息将纳入国家医保医用耗材分类与代码数据库,供各地医疗保障部门使用。
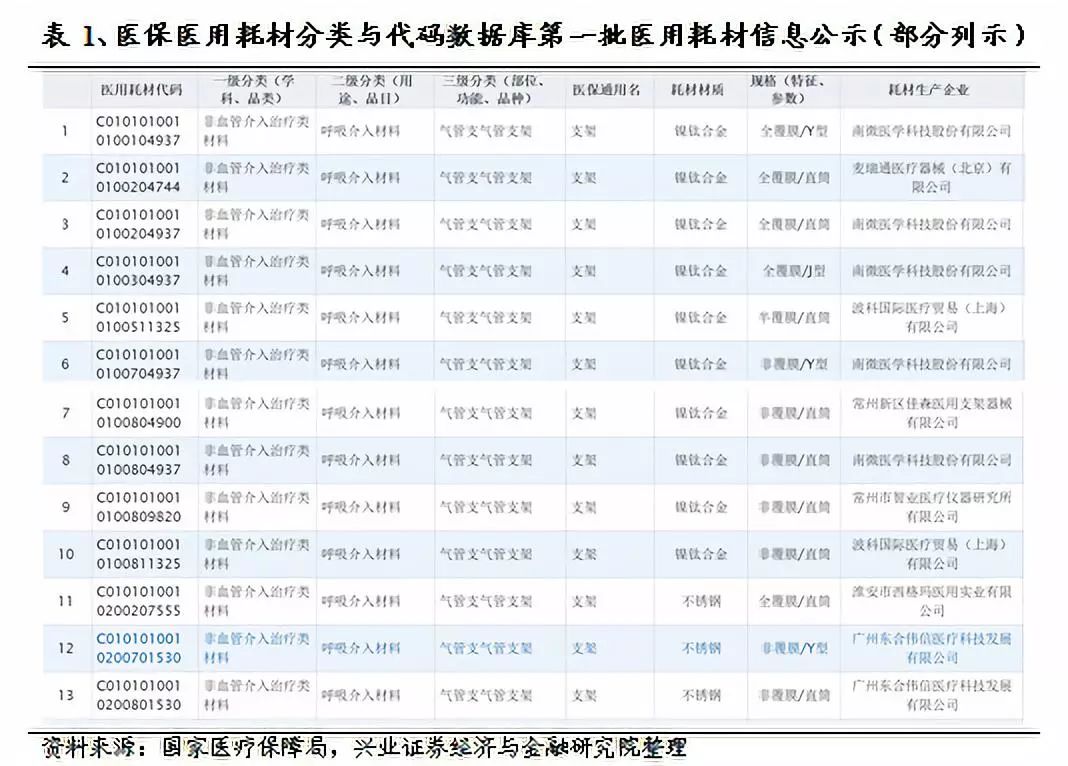
第一批医保医用耗材分类与代码公示,医保医用耗材全国统一编码如期推进。此次国家医保局发布的第一批医用耗材统一编码名单,首先是根据医用耗材学科、用途、部位、功能、品种,形成了17个一级分类(学科、品类)、176个二级分类(用途、品目)、1073个三级分类(部位、功能、品种),再根据耗材的材质、规格(特征、参数)以及生产企业进一步编码分类,包含共计30332种耗材,其中骨科材料的数量最多,高达18537种;其次为基础卫生材料达2970种;非血管介入治疗类材料、吻合器及附件、血管介入治疗类材料紧随其后,均达1000种以上。此次第一批医保医用耗材分类与代码公示,是对此前医保局发布的《国家医疗保障局关于印发医疗保障标准化工作指导意见的通知》(医保发〔2019〕39号)(以下简称《通知》)的阶段性成果落地。2019年6月27日,国家医疗保障局发布上述《通知》,提出为形成全国统一的医疗保障标准化体系,国家医保局明确从医保疾病诊断和手术操作、医疗服务项目、药品、医用耗材4项信息业务编码标准开始试点。到2020年,在全国统一医疗保障信息系统建设基础上,全面实现15项信息业务编码标准的落地使用,并同步发布了《医保疾病诊断和手术操作、药品、医疗服务项目、医用耗材四项信息业务编码规则和方法》。其中医保医用耗材编码分5个部分共20位,通过大写英文字母和阿拉伯数字按特定顺序排列表示:其中第1部分是耗材标识码,第2部分是分类码,第3部分是通用名码,第4部分是产品特征码,第5部分是生产企业码,其中第4部分和第5部分都是建立在“医疗器械唯一标识UDI”的基础上。

医疗器械唯一标识系统规则是医保高值医用耗材分类与编码的基础,满足医疗器械流通和使用环节精细化识别和记录的需求。医疗器械唯一标识(简称UDI)是医疗器械产品身份证,是医疗器械的“国际语言”。医疗器械唯一标识由产品标识和生产标识组成,产品标识是识别注册人/备案人、医疗器械型号规格和包装的唯一代码,是从数据库获取医疗器械相关信息的“关键字”,是唯一标识的必须部分;生产标识包括与生产的全部过程相关的信息,包括产品批号、序列号、生产日期和失效日期等,可与产品标识联合使用,满足医疗器械流通和使用环节精细化识别和记录的需求。作为国际通行做法,欧美等国家和地区均在积极地推进UDI系统。在我国,业界对此呼吁多年,建立UDI系统,为每一个医疗器械赋予身份证,打通从生产企业到流通、使用所有环节的编码、数据接口、电子数据交换等相关信息的接口,实现全国范围内、医疗器械全生命周期内信息可交换,实现生产、经营、使用各环节的透明化、可视化,提升产品的可追溯性,对于净化市场、优化营商环境、提升医疗服务的品质,助力医疗器械产业转型升级和健康发展将起到非消极作用。早在2018年2月27日,国家食品药品监督管理总局组织制定了《医疗器械唯一标识系统规则(征求意见稿)》;2019年7月1日,国家药监局综合司、国家卫生健康委办公厅联合印发《医疗器械唯一标识系统试点工作方案》;2019年10月14日,国家药监局印发了《关于做好第一批实施医疗器械唯一标识工作有关事项的通告》,该《通告》对第一批医疗器械唯一标识实施品种范围、进度安排、工作要求等进行了明确规定,根据《通告》,2020年10月1日起,生产列入首批实施目录的医疗器械,应当具有医疗器械唯一标识。第一批参与唯一标识系统试点的医疗器械企业包含外资和国产共计115家企业。
医保局旨在加强高值医用耗材规范化管理,建立高值医用耗材基本医保准入制度。2019年6月4日,国务院办公厅印发了《深化医药卫生体制改革2019年重点工作任务》,其中提到制定医疗器械唯一标识系统规则,逐步统一全国医保高值医用耗材分类与编码。对单价和资源消耗占比相比来说较高的高值医用耗材开展重点治理,改革完善医用耗材采购政策。随后,在2019年7月19日,国务院办公厅印发实施《治理高值医用耗材改革方案》(以下简称“方案”),该方案是对此前发布的《深化医药卫生体制改革2019年重点工作任务》中关于高值耗材部分的进一步深化和完善。方案指出,统一编码体系和信息平台,加强高值医用耗材规范化管理,将单价和资源消耗占比相比来说较高的高值医用耗材作为重点治理对象;制定医疗器械唯一标识系统规则,逐步统一全国医保高值医用耗材分类与编码,探索实施高值医用耗材注册、采购、使用等环节规范编码的衔接应用。从时间节点来看,制定医疗器械唯一标识系统规则以及逐步统一全国医保高值医用耗材分类与编码均将在2020年底前完成。同时,此次方案亦提出实行医保准入和目录动态调整,建立高值医用耗材基本医保准入制度,实行高值医用耗材目录管理,健全目录动态调整机制,及时增补必要的新技术产品,退出不再适合临床使用的产品。并且,类似于药品实施的政策,高值耗材亦将逐步实施医保准入价格谈判,实现“以量换价”。在医保支付政策方面,方案提出结合医保基金支付能力、患者承受能力、分类集中采购情况、高值医用耗材实际市场交易价格等因素,最大限度地考虑公立医疗机构正常运行,研究制定医保支付政策;科学制定高值医用耗材医保支付标准,并建立动态调整机制。针对已通过医保准入谈判的,按谈判价格确定医保支付标准;针对类别相同、功能相近的高值医用耗材,探索制定统一的医保支付标准。
医用耗材统一编码是耗材带量采购的实施基础,而耗材带量采购政策压力小于药品。我们大家都认为2020年是医保局高值耗材带量采购在更多省份落地的关键年份,而高值耗材和药品在产品属性和采购模式上存在众多不同。从产品属性来看,医疗器械没有“原研”和“仿制”区别,各类器械规格参数众多,难以进行“一致性”评价,质量分级只能通过临床数据、医生评价和产品材料来质量区分;而且一致性评价需要较长的周期,而耗材通常来说生命周期只有两年左右,厂家自己针对产品的频繁换代有几率会使一致性评价还没做完,新产品就上市了。从采购和使用来看,医疗器械的采购不仅要考虑产品的技术水平,更要考虑医生的使用习惯,更换品牌难度较大,所以招标对于器械的价格影响有限,品牌力强的企业具有定价能力。国家选择高值耗材进行带量采购,主要由于高值耗材单价较高,出厂价和终端价之间扣率较大,渠道中有较多“水分”,集采降价压力大部分由经销商承担,对于出厂价格影响较小。而从量的角度来看,市占率大的国产企业凭借和其他国产同类企业相比优异的产品质量,和外资产品相比的价格上的优势,带量采购中标的概率较大,从而有利于行业集中度的提升,国产有突出贡献的公司市占率的扩大。另外,值得一提的是,此次公布的第一批医保医用耗材编码中没有IVD试剂,IVD诊断试剂虽然总体规模与高值耗材相近,但集采难度相对高值耗材更大,这还在于IVD试剂不同于一般的耗材,部分品类的IVD试剂需要和仪器联用,而仪器有一定的更新周期。相较于进院价下调,我们大家都认为医保局对于IVD试剂耗材可能从收费目录着手,由于耗材的采购是不直接占用医保费用,直接占用医保的是检验费用,医保局可能从统一各省收费标准开始,然而这又是利好国产IVD企业的,由于试剂耗材属于医院的成本端,国产试剂价格比进口低一半以上,医院有动力采购国产试剂,有利于进口替代。
投资建议:整体看来,国家医保局推进医保医用耗材全国统一编码,旨在加强高值医用耗材规范化管理,探索实施高值医用耗材注册、采购、使用等环节规范编码的衔接应用;耗材领域探索实行医保准入和目录动态调整,建立高值医用耗材基本医保准入制度,实行高值医用耗材目录管理。我们大家都认为未来符合卫生经济学、具有明确临床诊疗价值的耗材有望受益,国产耗材由于具有性能好价格低优势,有望逐步抢占进口的市场占有率;拥有自主创造新兴事物的能力、业务多元化布局,或是单一产品具有高技术上的含金量和高的附加价值,在差异化竞争中有着非常明显的优势的国产有突出贡献的公司有望在行业集中度提升中受益。建议关注创造新兴事物的能力强、产品线丰富的耗材企业和IVD的细分龙头公司,耗材企业如A股的乐普医疗、大博医疗、凯利泰、南微医学、健帆生物,以及港股的威高股份、春立医疗、爱康医疗、微创医疗等;IVD企业如迈瑞医疗、安图生物、迈克生物、艾德生物、万孚生物等。
本报告所载资料的来源被认为是可靠的,但本公司不保证其准确性或完整性,也不保证所包含的信息和建议不可能会发生任何变更。本公司并不对使用本报告所包含的材料产生的任何直接或间接损失或与此相关的其他任何损失承担任何责任。
本报告的版权归本公司所有。本公司对本报告保留一切权利。除非另有书面显示,否则本报告中的所有材料的版权均属本公司。未经本公司事先书面授权,本报告的任何部分均不得以任何方式制作任何形式的拷贝、复印件或复制品,或再次分发给任何其他人,或以任何侵犯本公司版权的其他方式使用。没有经过授权的转载,本公司不承担任何转载责任。
报告中投资建议所涉及的评级分为股票评级和行业评级(另有说明的除外)。评级标准为报告发布日后的12个月内公司股票价格(或行业指数)相对同期相关证券市场代表性指数的涨跌幅,A股市场以上证综指或深圳成指为基准。
市场有风险,投资需谨慎。本平台所载内容和意见仅供参考,不构成对任何人的投资建议(专家、嘉宾或
其他兴业证券股份有限公司以外的人士的演讲、交流或会议纪要等仅代表其本人或其所在机构之观点),亦不构成任何保证,接收人不应单纯依靠本资料的信息而取代自身的独立判断,应自主做出投资决策并自行承担风险。根据《证券期货投资的人适当性管理办法》,本平台内容仅供兴业证券股份有限公司客户中的专业投资者使用,若您并非专业投资者,为保证服务质量、控制投资风险,请勿订阅或转载本平台中的信息,本资料难以设置访问权限,若给您造成不便,还请见谅。在任何情况下,作者及作者所在团队、兴业证券股份有限公司不对任何人因使用本平台中的任何内容所引致的任何损失负任何责任。
本平台所载内容不构成对具体证券在具体价位、具体时点、具体市场表现的判断或投资建议,不能够等同



